Tabel periodik adalah salah satu kajian dalam ilmu Kimia yang akan mempermudah proses identifikasi berbagai unsur kimia. Sebagaimana yang sudah diketahui, senyawa kimia begitu dekat dengan kehidupan dan bahkan hampir semua produk yang ada melibatkan senyawa kimia.
Contohnya pemanis, pewarna, pengental, pengawet dan lain sebagainya. Meskipun bukan merupakan unsur alami, namun berbagai unsur kimia dalam produk tersebut biasanya sudah dipastikan keamanannya.
Nah, supaya bisa memastikan keamanan unsur kimia yang dimasukkan dalam produk, maka kamu harus paham betul soal tabel ini. Lalu apa pengertian dan bagaimana cara membaca tabel periodik ini? Berikut ulasannya, sekalian simak dengan informasi terkait lainnya ya.
Pengertian Tabel Periodik

Singkatnya, tabel yang dimaksud dalam penjelasan kali ini merupakan tabel yang di dalamnya adalah urutan unsur yang sesuai dengan golongan serta periodenya. Semua unsur dalam tabel periodik tersebut akan ditulis dalam bentuk singkatan.
Sebagai contoh untuk besi, hanya akan ditulis FE atau Hidrogen yang hanya ditulis dengan huruf H dan sebagainya. Proses penamaan yang seperti ini didasarkan pada nama ilmiah dari setiap unsur. Contoh kalau Fe yang merupakan besi itu tadi aslinya adalah Ferrum.
Kemudian kalau emas akan dilambangkan dengan singkatan Cu yang berasal dari nama Cuprum dan sebagainya. Selain pengertian tersebut, tabel ini juga bisa dianggap sebagai susunan berbagai unsur kimia dengan berdasarkan nomor atomnya.
Tabel ini akan dimulai dari nomor atom yang paling rendah, yakni hidrogen. Artinya, kalau ada pertanyaan soal apa unsur pertama dalam tabel periodik, maka jawabannya adalah hidrogen tadi. Nah, akhir dari tabel ini adalah nomor atom paling tinggi yang dimiliki oleh oganesson.
Lalu, bagaimanakah rupa tabel unsur kimia ini? Kamu bisa memperhatikan gambar tabel periodik berikut ini.
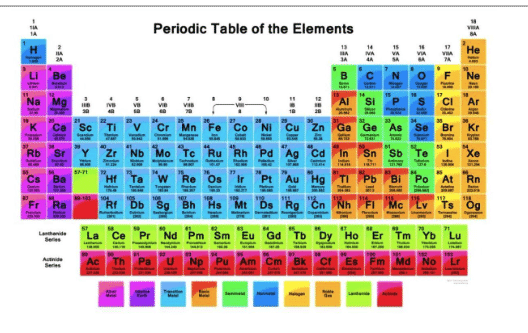
Struktur
Unsur-unsur yang dimuat dalam tabel ini terdiri atas 2 kelompok yaitu golongan dan periode. Golongan tabel periodik merupakan kelompok di lajur vertikal sedangkan untuk periode merupakan kelompok lajur horizontal.
1. Golongan
Golongan ini merupakan pengelompokan unsur yang didasarkan pada elektron valensi atau jumlah elektron yang ada pada kulit terluar. Kalau secara umum, golongan terbagi menjadi dua, ada golongan A dan ada golongan B.
Kalau golongan A, ini yang biasa disebut juga dengan golongan utama. Sementara kalau golongan B biasa disebut dengan golongan transisi. Kalau ditotal, semua golongan A dan B jumlahnya ada 18. Kalau dalam tabel unsur, maka semakin ke bawah jari-jari atomnya akan semakin besar.
Dengan kata lain, keelektronegatifan unsur akan menjadi semakin kecil. Penjelasan mengenai kedua golongan dalam tabel unsur ini sebagai berikut:
- Golongan A akan terdiri atas golongan IA, IIA, IIIA dan seterusnya hingga golongan VIIIA dengan penjelasannya sebagai berikut.
- Golongan I A yaitu logam alkali yang terdiri atas unsur-unsur dengan elektron valensi 1 dan yang termasuk dalam golongan ini ialah Fr, Cs, Rb, K, Na, Li dan H. Tetapi perlu diperhatikan, unsur H walaupun posisinya ada di golongan logam alkali, tetapi ini tidak termasuk logam ya. Golongan ini juga diketahui berada di blok s karena memang elektron valensinya yang ada di subkulit s
- Golongan II A yaitu logam alkali tanah ng terdiri atas unsur-unsur dengan elektron valensi 2 dan subkulit terakhirnya adalah s. Adapun unsur-unsur yang termasuk dalam golongan ini ialah Ra, Ba, Sr, Ca, Mg dan Be.
- Golongan III A yang terdiri atas unsur-unsur dengan elektron valensi 3 dan subkulit terakhirnya adalah p. Adapun unsur yang termasuk dalam golongan ini ialah Uut, TI, In, Ga, AI dan B
- Golongan IV A yang terdiri atas unsur-unsur dengan elektron valensi 4 dan subkulit terakhirnya adalah p. Adapun unsur yang termasuk dalam golongan ini ialahFI, Pb, Sn, Ge, Si dan C
- Golongan V A yang terdiri atas unsur-unsur dengan elektron valensi 5 dan subkulit terakhirnya adalah p. Adapun unsur yang termasuk dalam golongan ini ialah Mc, Bi, Sb, As, P dan N
- Golongan VI A yang terdiri atas unsur-unsur dengan elektron valensi 6 dan subkulit terakhirnya adalah p. Adapun unsur yang termasuk dalam golongan ini ialah Lv, Po, Te, Se, S dan O
- Golongan VII A yang biasa disebut juga dengan golongan halongen dan unsur yang termasuk dalam golongan ini ialahTs, At, I, Br, CI dan F
- Golongan VIII A atau yang biasa disebut juga dengan golongan gas mulia di mana susunan elektron valensinya sudah mencapai 8 atau mencapai kondisi oktet. Dengan kondisi ini, unsur ini sulit untuk bereaksi dengan unsur yang lainnya dan unsur yang termasuk dalam golongan ini ialah Rn, Xe, Kr, Ar, Ne dan He
- Golongan B yang terdiri atas I – VIII B pada umumnya terdiri atas unsur logam transisi dengan elektron valensi yang ada di subkulit d. Ini juga yang menjadi alasan kenapa kemudian golongan B ada di blok d.
2. Periode
Periode pada dasarnya merupakan kelompok unsur yang didasarkan pada banyaknya kulit atau tingkat energinya. Kalau kamu menemukan ada unsur yang kulit terahirnya 2, ini berarti unsur tadi tergolong unsur periode 2.
Kalau dalam satu periode, maka semakin ke kanan keelektronegatifan unsur akan semakin besar. Dengan kata lain, jari-jari atom akan semakin kecil kalau semakin ke arah kanan tabel.
3. Blok F
Selain ada golongan dan periode, ada juga blok f yang umum disebut dengan deret lantanida dan aktinida. Dalam deret ini terdapat unsur yang subkulit terakhinya adalah F. Adapun deret lantanida ini termasuk dalam golongan logam tanah jarang.
Bahkan dalam deret ini ada satu unsur yang bersifat radioaktif, namanya adalah prometium. Dalam deret ini akan ada 15 unsur yang beberapa diantaranya ialah prometium, neodimium, praseodimium, serium dan lantanum.
Sedangkan kalau deret aktinida berisi unsur yang hampir semuanya bersifat radioaktif. Sama seperti lantanida, dalam aktinida juga ada 15 unsur yang beberapa diantaranya adalah torium dan uranium, dua unsur yang sangat terkenal.
Unsur Tabel Periodik Beserta Namanya dan Simbolnya

Kalau ditanya soal ada berapa unsur dalam tabel periodik, jawabannya adalah 118 yang sudah diidentifikasi. Dari jumlah tersebut, 94 diantaranya ada di bumi secara alami dan sisanya adalah unsur sintetis. Adapun nama-nama unsur kimia yang dimaksud sebagai berikut:
1. Hidrogen: H
2. Helium: He
3. Lithium: Li
4. Beryllium: Be
5. Boron: B
6. Carbon: C
7. Nitrogen: N
8. Oxygen: O
9. Fluorine: F
10. Neon: Ne
11. Sodium: Na
12. Magnesium: Mg
13. Aluminum: Al
14. Silicon: Si
15. Phosphorus: P
16. Sulfur: S
17. Chlorine: Cl
18. Argon: Ar
19. Potassium: K
20. Calcium: Ca
21. Scandium: Sc
22. Titanium: Ti
23. Vanadium: V
24. Chromium: Cr
25. Manganese: Mn
26. Iron: Fe
27. Cobalt: Co
28. Nickel: Ni
29. Copper: Cu
30. Zinc: Zn
31. Gallium: Ga
32. Germanium: Ge
33. Arsenic: As
34. Selenium: Se
35. Bromine: Br
36. Krypton: Kr
37. Rubidium: Rb
38. Strontium: Sr
39. Yttrium: Y
40. Zirconium: Zr
41. Niobium: Nb
42. Molybdenum: Mo
43. Technetium: Tc
44. Ruthenium: Ru
45. Rhodium: Rh
46. Palladium: Pd
47. Silver: Ag
48. Cadmium: Cd
49. Indium: In
50. Tin: Sn
51. Antimony: Sb
52. Tellurium: Te
53. Iodine: I
54. Xenon: Xe
55. Cesium: Cs
56. Barium: Ba
57. Lanthanum: La
58. Cerium: Ce
59. Praseodymium: Pr
60. Neodymium: Nd
61. Promethium: Pm
62. Samarium: Sm
63. Europium: Eu
64. Gadolinium: Gd
65. Terbium: Tb
66. Dysprosium: Dy
67. Holmium: Ho
68. Erbium: Er
69. Thulium: Tm
70. Ytterbium: Yb
71. Lutetium: Lu
72. Hafnium: Hf
73. Tantalum: Ta
74. Tungsten: W
75. Rhenium: Re
76. Osmium: Os
77. Iridium: Ir
78. Platinum: Pt
79. Gold: Au
80. Mercury: Hg
81. Thallium: Tl
82. Lead: Pb
83. Bismuth: Bi
84. Polonium: Po
85. Astatine: At
86. Radon: Rn
87. Francium: Fr
88. Radium: Ra
89. Actinium: Ac
90. Thorium: Th
91. Protactinium: Pa
92. Uranium: U
93. Neptunium: Np
94. Plutonium: Pu
95. Americium: Am
96. Curium: Cm
97. Berkelium: Bk
98. Californium: Cf
99. Einsteinium: Es
100. Fermium: Fm
111. Mendelevium: Md
112. Nobelium: No
113. Lawrencium: Lr
114. Rutherfordium: Rf
115. Dubnium: Db
116. Seaborgium: Sg
117. Bohrium: Bh
118. Hassium: Hs
119. Meitnerium: Mt
120. Darmstadtium: Ds
121. Roentgenium: Rg
122. Copernicium: Cn
123. Ununtrium: Uut
124. Ununquadium: Uuq
125. Ununpentium: Uup
126. Ununhexium: Uuh
127. Ununseptium: Uus
128. Ununoctium: Uuo
Jenis-Jenis Unsur Pada Tabel Periodik
Tabel unsur memuat beragam jenis unsur baik itu non logam, logam post transisi, logam transisi, semilogam dan logam. Lalu, dari daftar unsur yang sudah disebutkan, bagaimana pembagiannya? Untuk itu, kamu bisa memperhatikan penjelasan berikut:
Unsur Logam
Unsur logam dalam tabel yang dimaksud akan terbagi menjadi empat, ada deret aktinida – lantanida, logam post transisi, logam transisi dan logam utama dengan penjelasannya sebagai berikut:
- Deret Lantanida dan Aktinida
Sesuai dengan yang sudah disebutkan sebelumnya, kedua deret ini masih termasuk logam walaupun laktanida adalah unsur yang lumayan jarang ditemukan. Padahal sebenarnya jumlah deret laktanida jumlahnya lumayan melimpah di bagian kerak bumi.
Bahkan tidak menutup kemungkinan juga kalau ke depannya laktanida ini akan dikembangkan di waktu mendatang. Sedangkan kalau aktinida berhubungan erat dengan nuklir, makanya kajiannya pun sulit dijangkau oleh kimia terapan.
- Logam Post Transisi
Logam pos transisi, posisinya ada di antara golongan unsur logam transisi dan metaloid. Jenis unsur logam yang satu ini memiliki titik didih dan tittik leleh yang relatif lebih rendah dibandingkan logam transisi dan sifatnya pun lebih lunak. Contohnya Ga, Al, Bi dan Pb.
- Logam Transisi
Ini adalah jenis unsur yang ada di golongan I B – VIII B dan biasanya ditandai oleh warna ungu. Logam transisi ini sifatnya lebih keras dan juga sulit untuk bereaksi karena elektron valensinya yang lebih banyak. Contoh yang bisa dengan mudah dikenali ialah besi.
- Logam Utama
Logam utama ada di golongan I A dan II A. Kedua golongan ini memiliki sifat reaktif karena elektron valensinya yang relatif lebih sedikit dari logam transisi. Kalau hendak dibandingkan pun, sifat logam ini lebih lunak dan titik leleh serta titik didihnya juga lebih rendah.
Unsur Semilogam
Unsur yang satu ini umumnya akan ditunjukkan dengan warna kuning keemasan dan unsur semilogam biasa disebut pula dengan metaloid. Semilogam memiliki sifat yang merupakan perpaduan antara non logam dengan logam.
Biasanya pula unsur-unsur yang tergolong dalam semilogam bisa dimanfaatkan sebagai bahan yang semi konduktor. Misalnya B atau boron, Ge atau germanium, Si atau silicon dan sebagainya.
Unsur Non Logam
Unsur non logam ialah unsur yang ada di golongan VII A (iodin, brom, klor dan fluor), VI A (selenium, sulfur dan oksigen), V A (fosfor dan nitrogen, IV A (karbon) dan I A (hidrogen) serta seluruh unsur yang ada di VIII A. Semua unsur dalam kategori ini mudah berikatan dengan unsur yang lainnya.
Cara Baca Tabel Periodik
Untuk membaca tabel unsur-unsur kimia, kamu bisa mengawalinya dari kiri atas sampai ke bagian kanan bawah. Perlu diingat, unsur kimia yang posisinya ada di kiri atas adalah unsur kimia yang nomor atomnya paling kecil.
Sedangkan untuk unsur kimia yang posisinya di bagian kanan hingga ke bawah adalah unsur kimia yang nomor atomnya lebih besar. Nah, nomor atom itu adalah angka yang dimulai dari angka 1 hingga angka 118 dan nomor ini merupakan jumlah proton yang dimiliki unsur.
Cara Menghafal Tabel Periodik
Untuk kamu yang ingin menghafalkan nama-nama unsur dalam tabel yang dimaksud, bisa melakukannya dengan cara membuat susunan kalimat singkat yang terdiri atas simbol-simbol nama unsur. Biasanya, cara ini sangat efektif dan mempermudah banyak orang untuk mengingatnya.
Ambil contoh kamu ingin menghafal unsur yang ada di golongan I A. Seperti yang bisa dilihat dalam gambar di atas, golongan I A ini terdiri atas unsur H, unsur Li, unsur Na, unsur K, unsur Rb, unsur Cs dan unsur Fr.
Simbol-simbol unsur tadi bisa dirangkai menjadi kalimat seperti Hari Libur Nanti Ku Rebut Cinta si Frido. Hal yang sama bisa kamu lakukan pada golongan yang lain, dan pastinya kamu harus menghafal maksud dari simbol-simbol tersebut juga ya.
Sudah lebih paham dengan tabel periodik? Sekarang, coba perhatikan gambar tabel yang tercantum di atas dan cobalah buat kalimat dari rangkaian simbol unsur-unsur agar kamu bisa segera menghafalnya.
Baca Juga: