Dalam perkembangan listrik, terdapat beberapa tokoh penting yang berperan di dalamnya. Michael Faraday merupakan ilmuwan yang pertama kali menemukan generator listrik sekaligus penggagas Hukum Faraday. Penemuannya tersebut berhasil digunakan masyarakat dunia hingga saat ini.
Sosok Faraday dan hukumnya tentu tidak asing lagi dalam mata pelajaran Fisika maupun Kimia. Dalam penemuan tersebut, dijelaskan terkait aspek kuantitatif (massa zat, jumlah mol elektron, dan volume gas) yang ada pada elektrolisis dan akhirnya menghasilkan 2 hukum elektrolisis Faraday.
Bagi kamu yang sedang menimbah ilmu science, pasti akan mempelajari hukum-hukum yang telah ditemukan Faraday. Untuk menguasai pembahasan tersebut, dalam artikel ini akan dibahas tentang pengertian, rumus, penerapan, contoh soal, dan masih banyak lagi.
Pengertian Hukum Faraday

Pada dasarnya, Faraday’s Law merupakan hukum yang menunjukkan hubungan antara massa suatu zat dengan jumlah listrik, baik di katoda maupun anoda dalam proses elektrolisis. Nama hukum ini diambil dari penemunya yaitu Michael Faraday, seorang ilmuwan fisika dan kimia asal Inggris.
Faraday’s Law berhasil menjadi salah satu hukum yang paling banyak berpengaruh dalam perkembangan listrik. Banyak ilmuwan lain yang turut menemukan alat atau hukum baru dengan mengembangkan hukum yang telah ditemukan oleh Michael Faraday sebelumnya.
Mempelajari hukum ini tergolong cukup penting bagi kamu yang sedang menuntut ilmu atau berkecimpung di bidang fisika, kimia, hingga kelistrikan. Selain itu, penerapan Faraday’s Law juga banyak ditemukan di bidang industri, salah satunya dalam memproduksi alat-alat kimia.
Prinsip Dasar Hukum Faraday
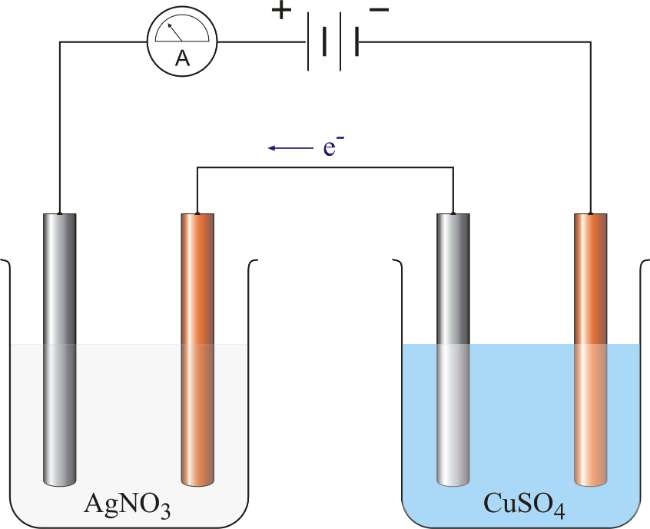
Setelah memahami pengertian dari Faraday’s Law, selanjutnya kamu juga wajib mengetahui bagaimana prinsip dasarnya. Selama proses elektrolisis, Michael Faraday mengamati bahwa setiap atom dihasilkan dibawa oleh satu mol elektron.
Dalam hasilnya, terdapat konstanta yang dapat digunakan untuk menghitung besarnya muatan yang ada di dalam satu mol elektron. Hasil ini juga bermanfaat untuk memudahkan perhitungan stoikiometri dalam kimia tanpa harus menghitung muatan elektron setiap saat.
Selain itu, Faraday’s Law juga digunakan saat membuat hipotesis tentang bagaimana interaksi medan magnet dengan rangkaian listrik. Dalam percobaan ini juga ditemukan munculnya gaya gerak listrik (ggl) yang juga dikenal sebagai induksi elektromagnetik.
Bunyi Hukum Faraday
Faraday’s Law terdiri dari 2, yaitu hukum pertama dan kedua. Kedua hukum tersebut memiliki bahasan serta rumus yang berbeda-beda. Nah, untuk mengetahui lebih lanjut terkait hukum pertama maupun kedua dari Faraday, bisa melihat uraian berikut ini dengan lengkap.
1. Hukum Faraday I
Faraday’s Law yang pertama menyatakan bahwa massa zat yang diendapkan maupun dilarutkan akan sebanding dengan jumlah muatan listrik yang mengalir dalam proses elektrolisis. Dalam hal ini, semakin banyak jumlah massa zat yang larut atau mengendap maka muatan listriknya juga semakin besar.
Sebaliknya, jika jumlah massa zat sedikit, maka muatan listrik yang dihasilkan pun akan kecil. Oleh karena massa zat disimbolkan dengan W dan muatan listrik sebagai Q, maka dapat disimpulkan bahwa W Q. Dengan demikian, rumus Faraday I menjadi:
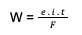
Dimana:
W : Massa zat yang dihasilkan (gram)
e : Ekuivalen
I : Kuat arus listrik (A)
t : Waktu (s)
F : Tetapan Faraday dengan nilai 96.500 Coulomb
2. Hukum Faraday II
Berbeda dengan hukum yang pertama, Faraday’s Law II menjadi lebih menarik karena berlaku pada 2 sel elektrolisis dengan zat yang berbeda. Perbedaan jumlah dari 2 zat yang berbeda akan menyebabkan massa ekuivalen berbanding lurus dengan zat-zat tersebut.
Artinya, hukum kedua Faraday ini menjelaskan bahwa massa zat yang dihasilkan dari proses elektrolisis sebanding dengan massa ekuivalennya. Jika sel elektrolisis terdiri dari arus dan muatan listrik yang sama, maka perbandingan massa zat dan massa ekuivalen juga akan sama.
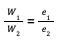
W1 : Massa zat 1 (gram)
W2 :Massa zat 2 (gram)
e1 : Ekuivalen zat 1
e2 : Ekuivalen zat 2
Hukum kedua Faraday ini menegaskan bahwa penerapannya dapat digunakan untuk menghitung aspek kuantitatif dari zat-zat yang berperan dalam proses elektrolisis. Selain itu, Michael Faraday juga menerapkan hukum tentang induksi elektromagnetik setelah percobaannya.
Aplikasi Hukum Faraday Dalam Kehidupan Sehari-Hari
Mempelajari hukum yang telah dikemukakan oleh Faraday tidak hanya digunakan untuk menjawab soal dalam mata pelajaran kimia dan fisika. Akan tetapi, penerapan hukum ini dapat dilihat pada beberapa alat yang sering ditemukan atau bahkan digunakan sehari-hari seperti berikut ini.
1. Generator Listrik
Pemanfaatan Faraday’s Law yang pertama adalah pada generator listrik. Alat ini dibuat pertama kali menggunakan konsep yang sudah ditemukan Faraday dan berhasil mendapat banyak perhatian. Bahkan, beberapa ilmuwan selanjutnya mencoba untuk mengembangkan generator listrik.
Prinsip kerja dari generator listrik yaitu bagaimana induksi elektromagnetik mampu menghasilkan arus listrik. Kumparan yang berputar di dalam medan magnet menyebabkan terjadinya perubahan fluks magnetik. Akibatnya, perubahan tersebut menginduksi arus listrik yang muncul dalam kumparan.
2. Transformator Listrik
Penerapan kedua dari Faraday’s Law yang juga sering ditemui dalam kehidupan sehari-hari transformator listrik. Alat ini berfungsi untuk mengubah tegangan listrik dari satu tingkat ke tingkat yang berbeda. Prinsip yang digunakan transformator untuk bekerja adalah induksi elektromagnetik.
Perubahan arus listrik yang terjadi di dalam kumparan akan menyebabkan perubahan fluks magnetik. Dengan prinsip yang sama dengan generator sebelumnya, fluks magnetik yang berubah akan menginduksi arus listrik yang ada di kumparan lainnya.
3. Produksi Zat (Bahan) Kimia
Dalam industri, bahan atau zat kimia seringkali dibutuhkan dalam membuat berbagai hal terutama dalam laboratorium. Zat-zat tersebut dibuat melalui proses elektrolisis, seperti hidrogen, gas klorin, dan gas oksigen. Jadi, prinsip kerja dari Faraday’s Law memudahkan pembuatan zat-zat kimia tertentu.
Akan tetapi, perlu diketahui bahwa tidak semua zat atau bahan kimia dihasilkan dari prinsip Faraday. Beberapa zat kimia juga diperoleh dari bahan-bahan alami seperti asam jeruk, garam, atau gula tebu. Selain itu, juga terdapat zat kimia sintetik, misalnya nilon, karet, plastik, dan polyester.
4. Elektrolisis
Reaksi redoks dalam proses kimia yang dipicu oleh arus listrik melalui larutan elektrolit dikenal sebagai elektrolisis. Dalam hal ini, Faraday’s Law berfungsi untuk menghubungkan jumlah zat yang terbentuk atau terurai dengan besar arus listrik yang mengalir selama proses elektrolisis.
Dalam sel elektrolisis terdapat larutan elektrolit yang mengandung ion bebas, sumber arus listrik, serta 2 elektroda yaitu katoda dan anoda. Katoda merupakan elektroda yang mengalami reduksi (-), sedangkan anoda adalah elektroda yang mengalami oksidasi (+).
5. Mikrofon
Kamu tentu tidak asing lagi dengan mikrofon. Alat yang dapat mengubah gelombang suara menjadi sinyal listrik. Dalam kehidupan sehari-hari, mikrofon digunakan sebagai alat pengeras suara sehingga bisa didengar oleh orang lain dengan jelas dalam suatu tempat, baik ruang terbuka atau tertutup.
Di dalam mikrofon, gelombang suara yang dikeluarkan manusia akan diubah menjadi getaran mekanik. Getaran tersebut kemudian mengubah kumparan yang ada di dalam mikrofon dan menginduksi arus listrik yang mewakili sinyal suara.
6. Pemurnian Logam Kotor
Logam merupakan unsur kimia yang memiliki sifat yang keras dan kuat. Untuk digunakan dalam pembuatan alat atau campuran zat tertentu, unsur kimia ini harus dimurnikan terlebih dahulu melalui proses elektrolisis. Nah, dalam proses inilah digunakan gagasan dari Michael Faraday.
Pemurnian logam dilakukan dengan menyiapkan 2 buah logam, logam kotor yang berfungsi sebagai anoda dan logam murni yang berfungsi sebagai katoda. Kedua logam tersebut disusun dalam larutan elektrolisis CuSO4. Dari proses pemurnian logam kotor, akan dihasilkan logam tunggal yang murni.
7. Penyepuhan Logam
Meskipun termasuk dalam material yang kuat, namun logam masih rentan terhadap korosi. Saat unsur ini terkena air yang menyebabkan terjadinya reaksi elektrokimia sehingga memicu terjadinya korosi. Oleh karena itu, dibutuhkan cara untuk melindungi logam yaitu dengan penyepuhan.
Proses penyepuhan logam adalah pemberian lapisan agar material tersebut lebih tahan dan tidak mudah terpengaruh reaksi elektrokimia. Selain itu, penyepuhan juga dapat memperindah tampilan dari sebuah logam. Misalnya, alat-alat makan dari logam yang disepuh menggunakan emas atau perak.
8. Motor Listrik
Penerapan selanjutnya dari Faraday’s Law adalah motor listrik. Alat ini memiliki prinsip yang berlawanan dengan generator listrik. Rotasi rotor didorong oleh gaya yang dihasilkan oleh arus listrik yang mengalir ke dalam medan magnet. Prinsip ini menggunakan 2 hukum yaitu, Lenz dan Faraday.
Hukum Lenz menyatakan bahwa jika gaya gerak listrik induksi (ggl) timbul dalam suatu rangkaian, maka arah arus induksinya akan menentang penyebab dari efek tersebut. Akibatnya, tandanya berubah menjadi negatif (-). Hukum ini hanya berlaku pada rangkaian tertutup.
Contoh Soal Hukum Faraday
1. Jika arus listrik sebesar 20 A dialirkan selama 10.000 detik ke dalam larutan CuSO4, hitunglah massa tembaga yang dihasilkan! (Ar Cu = 63,5).
Jawab:
Diketahui:
Ar Cu = 63,5
I = 20 A
t = 10.000 s
Ditanyakan: massa tembaga?
Penyelesaian:
Reaksi Pengendapan Tembaga (Cu):

Jadi, massa tembaga (Cu) yang dihasilkan dalam proses tersebut adalah 65,803 gram.
2. Hitunglah waktu yang dibutuhkan untuk mengendapkan 8 gram besi dalam larutan besi (III) klorida dengan kuat arus 4 A? (Ar Fe = 55,85)
Jawab:
Diketahui:
G = 8 gr
I = 4 A
Ar Fe = 55,85
Ditanyakan: waktu (t)?
Penyelesaian:
Reaksi pada katoda:

Jadi, waktu yang dibutuhkan untuk mengendapkan 8 gram besi (Fe) dalam reaksi tersebut adalah 10.367,42 detik.
Hukum Faraday adalah teori yang dikemukakan oleh ilmuwan fisika dan kimia asal Inggris yaitu Michael Faraday. Teori Faraday ini terbagi menjadi 2, yaitu hukum I dan II yang banyak diterapkan dalam kehidupan sehari-hari. Misalnya, pembuatan generator listrik, mikrofon, elektrolisis, dan lainnya.
Baca Juga: